保養的流程不複雜,掌握劑型的關鍵由水相到油相,液體到固體產品的使用原則,抓住這個準則,市場上眾多的保養品就都難不倒您了。
正確的臉部保養順序
早上保養順序
清潔(洗臉) > 爽膚(化妝水) > 補充性保養品(保濕or精華液) > 滋養(乳液) > 日霜(取決於個人需求) > 防曬隔離霜
夜晚保養順序
清潔(卸妝+洗臉) > 去角質 > 面膜 > 爽膚(化妝水) > 補充性保養品(保濕or精華液) > 滋養(乳液) > 晚霜(取決於個人需求)
- 去角質:混和性肌膚最多1周2次;乾性肌膚最多1周1次
- 面膜:面膜有各式各樣的使用方法,有些可以天天使用,有些則不適合,使用前請參閱包裝說明
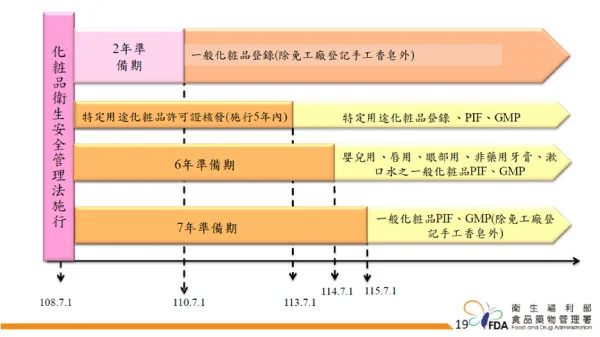
依據「化粧品衛生安全管理法」第4條規定:「經中央主管機關公告之化粧品種類及一定規模之化粧品製造或輸入業者應於化粧品供應、販賣、贈送、公開陳列或提供消費者試用前,完成產品登錄及建立產品資訊檔案;其有變更者,亦同。」
「化粧品產品登錄辦法」已於108年7月1日施行,一般化粧品自110年7月1日起,完成產品登錄的化粧品將不得供應、販賣、贈送、公開陳列或提供消費者試用。
108 年 5 月 30 日衛生福利部食品藥物管理署公告「化粧品產品資訊檔案管理辦法」及「應建立產品資訊檔案之化粧品種類及施行日期」,113 年 6 月 30 日前有效之「特定用途化粧品」許可證將於隔日立即失效,改由「產品資訊檔案」(簡稱 PIF)取代之。
113 年 7 月 1 日起,化粧品將依照產品類別分三階段開始實施,舉凡化桩品販賣、贈送、公開陳列或試用,均需依產品類別依時程陸續完成「產品資訊檔案」。
資訊來源:
https://www.fda.gov.tw/TC/siteList.aspx?sid=10992
https://www.fda.gov.tw/TC/siteContent.aspx?sid=12524
https://www.fda.gov.tw/tc/includes/GetFile.ashx?id=f637018029906273690&type=2&cid=30721
保養品代工類型:
OEM:
客戶已有「既有的產品」或是「預計的配方與包裝設計」,產品從頭到尾都已有概念,便可以請吉立伊貝單純負責OEM(從產品內容物的生產製造到充填、包裝、品檢、出貨),建議OEM客戶或多或少要對原料有一定的了解並有自己的通路、市場與產品的獨特賣點(USP)。
ODM:
對於通路市場也有自己的想法,但對於保養品詳細內容只了解部分的客戶,需要委託代工廠代為提供包材、內料、設計、包裝等部分的建議與設計協助,提供及整合產品資訊即為ODM的範疇。
OBM:
針對規劃自創品牌的企業客戶,有通路想開發保養品產業,且”有一組專業的團隊顧問”不論是外聘的顧問團或是公司內部的專業團隊,那就是屬於OBM的範疇,一般來說OBM是以提案的方式,再由公司內部做討論通過或是否決的方式進行。
我們會針對您的通路需求、預算等為您提供最適合的代工產品,更可以針對您的市場需求與品牌定位提供相關的建議。
如有任何代工相關的疑問,歡迎留言或連繫我們喔!
只要您有心想要加入保養品產業,或者您有新奇的產品構思與想法,不管您是直播主、YOUTUBER、網路賣家、SPA店店長、貿易商、青年創業、店商平台、團購主或公司企業,我們都可以為您打造符合您需求的產品喔!
一、產品登錄號碼。
二、產品中、英文名稱。但國產化粧品,得免登錄英文名稱。
三、產品種類及用途。
四、產品類型;其為系列產品者,應填列型號或色號。
五、產品劑型。
六、產品使用注意事項。
七、產品製造或輸入業者之名稱、地址及電話號碼。
八、產品製造場所之名稱、地址、國別及其符合化粧品優良製造規範情形。
九、產品全成分名稱。中央主管機關訂有使用限量之成分,並應以重量或容量百分比填列其含量。
十、產品其他有關說明。
前項登錄,應以中文、英文、號碼或國際通用符號為之。
化粧品產品資訊檔案(Product Information File, PIF)是與該上市產品相關的資料蒐集及整理,內容包含產品基本資料、製造場所符合化粧品優良製造準則、包裝標示、技術性相關資料及安全資料簽署人員審核的安全評估報告等,產品如含有公告的特定成分應符合使用限量規定,或具有特定的功能宣稱者則應有相關的測試報告。
化粧品產品資訊檔案,應以中文或英文建立下列資料:
一、產品基本資料:產品名稱、產品類別、劑型、用途、製造
廠名稱與地址及產品製造或輸入業者資訊。
二、完成產品登錄之證明文件。
三、全成分名稱及其各別含量。
四、產品標籤、仿單、外包裝或容器。
五、製造場所符合化粧品優良製造準則之證明文件或聲明書。
六、製造方法、流程。
七、使用方法、部位、用量、頻率及族群。
八、產品使用不良反應資料。
九、產品及各別成分之物理及化學特性。
十、成分之毒理資料。
十一、產品安定性試驗報告。
十二、微生物檢測報告。
十三、防腐效能試驗報告。
十四、功能評估佐證資料。
十五、與產品接觸之包裝材質資料。
十六、產品安全資料:
(一) 經安全資料簽署人員簽名並載明日期之安全性評估結
論及建議。
(二)安全資料簽署人員符合第四條至第六條規定之資格證
明文件。
資料來源:https://www.fda.gov.tw/TC/siteContent.aspx?sid=12524
因應化粧品衛生安全管理法第五條第七項規定,同條第一項及第二項有關特定用途化粧品之規定,於中華民國一百十三年七月一日停止適用。原「特定用途化粧品成分名稱及使用限制表」之規定,將納入「化粧品成分使用限制表」及「化粧品防曬劑成分使用限制表」,爰辦理廢止事宜,預定自中華民國一百十三年七月一日生效。
資訊來源:https://www.fda.gov.tw/tc/newsContent.aspx?cid=5072&id=30316
依據化粧品衛生安全管理法第7條規定,化妝、保養品外包裝或容器,應明顯標示
一、品名。
二、用途。
三、用法及保存方法。
四、淨重、容量或數量。
五、全成分名稱,特定用途化粧品應另標示所含特定用途成分之含量。
六、使用注意事項。
七、製造或輸入業者之名稱、地址及電話號碼;輸入產品之原產地(國)。
八、製造日期及有效期間
或 製造日期及保存期限
或 有效期間及保存期限
以上擇一標示即可。
九、批號。
十、其他經中央主管機關公告應標示事項。
前項所定標示事項,應以中文或國際通用符號標示之。但第五款事項,得以英文標示之。
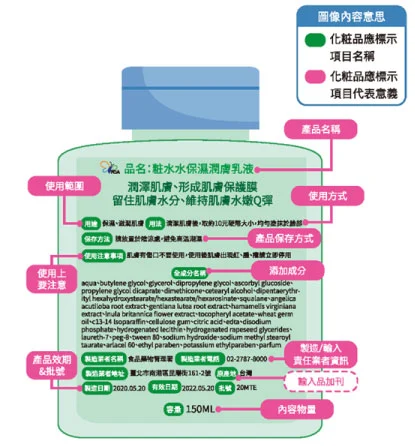
資訊來源:https://www.fda.gov.tw/tc/includes/GetFile.ashx?id=156&mid=137
化妝品標示範例轉載至TFDA會粧不會裝
應刊載標示事項,其中文字體大小規格如下:
產品內容物淨重或容量大於800g/800mL 者,其字體大小規格(高度或寬度)不得小於2.0mm(電腦字體5.5 號字)
淨重或容量小於(含)800g/800ml 大於300g/300ml 者,其字體大小規格(高度或寬度)不得小於1.6mm(電腦字體4.5 號字)
淨重或容量小於(含)300g/300mL大於 80g/80mL 者,其字體大小規格(高度或寬度)不得小於1.2mm(電腦字體3.5 號字)
淨重或容量小於(含)80g/80mL 者,不在此限。
資訊來源:https://www.fda.gov.tw/tc/includes/GetFile.ashx?id=f636694200420898195